警惕活动期血管炎患者的腹部体征
主诉 病史
男性,43岁,工人。因“间断鼻出血三个月”为主诉就诊于我院风湿免疫科病房。1个月前出现咳嗽咳痰,痰中带血,2周前出现周身紫癜,3天前出现腹泻及口腔溃疡。
查体 辅查
入院时,生命体征平稳,体温37.2度。查体:皮肤多发紫癜,心音清晰无杂音。肺部听诊可闻及少量湿罗音。腹部查体无特异性阳性体征。
诊断 处理
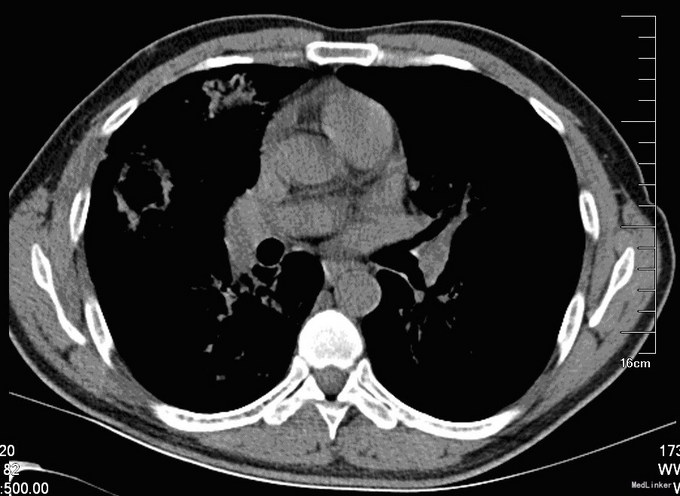
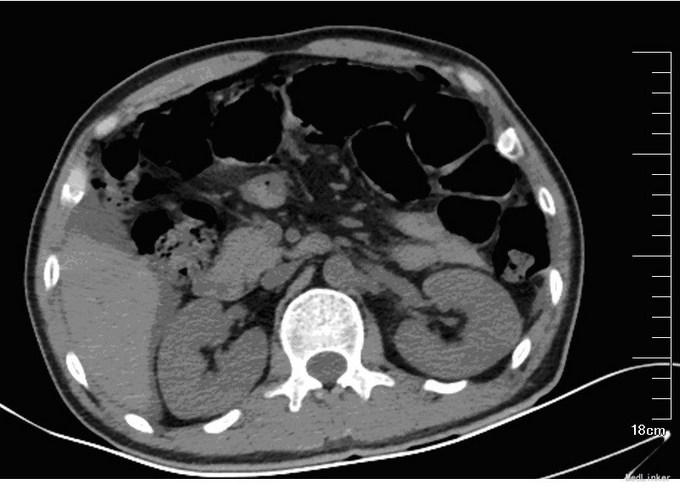
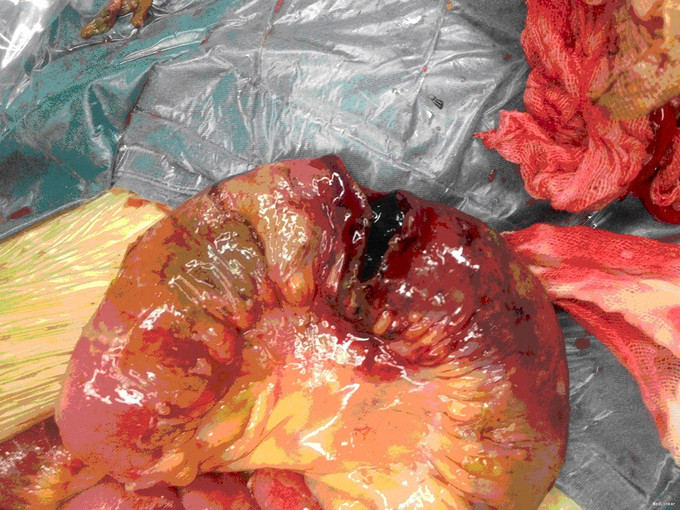
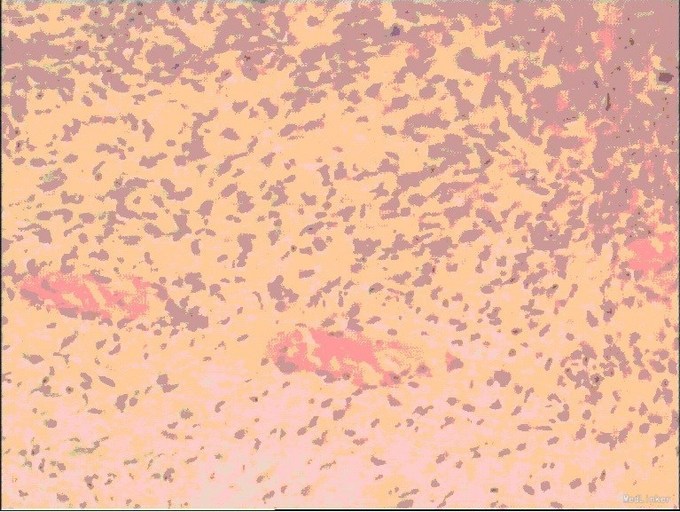
入院后,化验:血常规:白细胞:15600/mm3,嗜酸性粒细胞分数:20.3%; ESR 69 mm, CRP 176 mg/l,风湿因子:656 UI/ml,pANCA antibodies 阳性. 行肺CT:见双肺多发呈类圆形内部稍低密度影,大小不一,较大者约3.2*2.6cm(图1)。考虑肺泡出血和嗜酸性粒细胞侵润。鼻黏膜活检病理证明大量嗜酸性粒细胞侵润。根据上述,诊断为嗜酸性肉芽肿性多血管炎(EGPA,eosinphilic granulomatosis with polyangiitis)。予激素和免疫抑制剂等对症治疗。患者激素减量过程中出现咳血反复,周身及肛周出现溃疡破溃,再次与甲强龙500mg冲击后症状缓解,口腔及肛周、下肢溃烂均较前好转。进食软食一天后突然出现腹痛、发热,腹膜炎症状,查体:全腹压痛,以下腹部为重,伴有反跳痛及肌紧张。完善全腹CT检查考虑消化道穿孔(图2),EGPA并发穿孔的患者行剖腹探查,小肠穿孔修补术。术中见:腹腔小肠肠管明显扩张,多处脓苔,广泛粘连,腹腔内黄绿色渗出100ml,吸尽渗出探查,见距回盲部5cm至距TREITZ韧带150cm之间小肠多发穿孔共11处,较大者破孔3cm*3cm(图3),较小者0.4*0.4cm,予以4-0可吸收线沿肠壁横轴缝合肠壁全层及浆肌层。病理(图4):(小肠穿孔周缘)炎性肉芽组织。术后予以禁食水抗炎补液抑酸及激素治疗。术后6天因血管炎病情反复发作,出现发热,皮肤红斑,7天出现肠瘘,予以双腔套管持续冲洗接负压吸引后逐步愈合后出院。继续风湿免疫科随诊治疗。未有再次发生消化道穿孔。
随访 讨论
血管炎(vasculitis)是一类风湿免疫疾病,是以血管的炎症与破坏为主要病理改变的一组异质性疾病,其临床表现因受累血管的类型、大小、部位及病理特点不同而表现各异。目前主要根据受累血管的大小对血管炎进行了命名和定义(Chapel Hill会议关于系统性血管炎的命名及其定义)。分为三类。第一类大血管的血管炎分为巨细胞动脉炎和大动脉炎,第二类为中等大小血管的血管炎分为结节性多动脉炎和川崎病,第三类为小血管的血管炎,曾经分为韦格纳肉芽肿(Wegener’s granulomatosis ,WG),变应性肉芽肿性血管炎(Churg-Strauss syndrome,CSS),显微镜下多血管炎,现在新的分类统称为嗜酸性肉芽肿性多血管炎。 嗜酸性肉芽肿性多血管炎,是以过敏性哮喘。嗜酸性粒细胞增多、发热和全身性肉芽肿血管炎为特征的疾病,其病理特点是坏死性血管炎,组织中嗜酸性粒细胞侵润和结缔组织肉芽肿形成。此外,系统性红斑狼疮(systemic lupus erythematosus, SLE)、类风湿关节炎、肿瘤、感染,药物等也常出现血管炎,为继发性血管炎。 血管炎累及全身多个脏器及器官,可同时合并有肺部疾患,肾功能不全,消化道缺血溃疡等。消化道受累常见于EGPA,表现为嗜酸性粒细胞性胃肠炎,以腹痛,腹泻及消化道出血常见,嗜酸性粒细胞还可侵犯浆膜引起腹膜炎。变应性肉芽肿性血管炎(CSS)患者中几乎31%消化道受累,这是已知的预后不佳的因素之一。其中小肠受累占53.5%,大肠受累占29.11%,胃十二指肠受累占16.6%,胰腺炎和胆囊炎发生率为6.3%。死亡率是11.9%。 尽管在CSS患者中,消化道溃疡性病变是常见的,但溃疡穿孔是相对罕见的,仅有有限数量的病例被报道过。 活动期血管炎导致消化道穿孔的原因分析是由于胃肠道的小血管炎和血栓形成造成缺血所致。小肠是最常发生的部位。EGPA病变的典型的病理改变为:组织及血管壁大量的嗜酸性粒细胞浸润,血管周围的肉芽肿形成以及节段性纤维素样坏死性血管炎。另一方面,血管炎的治疗方案主要是激素治疗,合并免疫抑制剂。病情加重时予以免疫球蛋白冲击治疗或行血浆置换。病程长,易反复,需要长期大剂量的激素,本身也带来多种并发症。免疫抑制剂和小肠穿孔在血管炎的病程中关系并不清楚。但研究显示免疫抑制治疗,尤其适用皮质激素类,可能在小肠穿孔的病程中发挥作用。但有时临床也很难鉴别,小肠穿孔是由血管炎本身导致,还是高剂量的免疫抑制剂造成的。 血管炎患者合并消化道穿孔的治疗上,在非病情活动期的患者,急腹症常与风湿免疫性疾病无关,恰当的手术是合适的,早期手术有较好的预后。而活动期血管炎的消化道穿孔患者临床特点可能比较复杂。需要指出的是血管炎可累及全身多个系统,患者一般情况差,长期服用激素及免疫抑制剂,糖皮质激素可抑制机体的免疫功能,且无抗菌作用,长期应用常可诱发感染或加重感染,而且用糖皮质激素时患者往往自我感觉良好,掩盖感染发展的症状,以致腹膜刺激征常不典型。该患者无明显发热,穿孔后都有腹痛加重剧烈的主诉,查体板状腹并不明显,无全腹腹肌紧张,但穿孔处的肠管的腹膜炎很明确。在临床上,如果遇到血管炎活动期,大量运用激素的患者突发腹痛的主诉时,不要漏诊穿孔的可能性。 活动期血管炎并发消化道穿孔的治疗。目前,临床上并无统一定论和治疗策略。血管炎本身无有效根治疗法,对于并发消化道穿孔的患者手术切除局部并未改变血管炎本身的自然病程。激素,免疫抑制剂等虽可减轻症状,但减量或停药后易复发,而且大量激素对手术不利,易诱发或加重溃疡,在治疗上存在矛盾。因此目前治疗主要为综合治疗,预防复发。 对于血管炎导致的消化道穿孔,有医生倾向于保守治疗,继续系统用药,认为血管炎导致的消化道穿孔,病因源自自身免疫性疾病,外科治疗属于有创治疗,缝合的肠管可能不愈合,仍不能控制病情的发展,可能有再发穿孔的危险。建议继续系统用药,控制原发病,达到穿孔自愈。目前消化道穿孔后的外科治疗仍是经验性治疗,文献报道手术治疗后极易复发。外科手术治疗需慎重。坚决杜绝因误诊而实施的相关手术,为降低术后并发症发生率,应尽量避免在急性期进行外科手术治疗。当然,若发生消化道穿孔、出血等并发症,病死率极高,需及早诊断并急诊手术治疗。另也有文献报道切除范围与术后复发无明显关联,因为多数肠道损害多可自行恢复或在药物治疗下好转。 对于活动期血管炎临床诊断明确的消化道穿孔患者,我们倾向于积极外科干预,手术治疗。我们认为,消化道穿孔虽然为自身免疫性疾患,但已然形成的穿孔通过内科保守治疗,即使病情控制,也很难自行穿孔愈合,需要积极的外科手术干预。手术方式选择:一是行消化道穿孔修补术,二是行肠切除肠吻合术。多处穿孔患者如累及肠管范围过大,考虑切除肠管后出现短肠综合征,可予以一一修补,但术后肠瘘的风险加大。对于单发的穿孔,破口巨大,周围肠管只要无明确的缺血坏死表现,可行肠切除肠吻合术。该患者穿孔处达
